[이슈밸리=박지영 기자] 가상·증강현실 기술이 적용된 의료기기의 허가·심사가 쉬워질 전망이다.
식약처는 가상현실 또는 증강현실 기술이 적용된 의료기기가 점차 증가함에 따라 ’가상·증강현실 의료기기‘에 대한 안전성 검증 방법을 개선하고 임상시험 대상을 명확히 하는 내용을 반영해 ’의료기기의 허가·심사 가이드라인‘을 개정했다고 30일 밝혔다.
이번 개정의 주요 내용은 가상·증강현실 의료기기 소프트웨어 등 심사 대상, 임상시험이 요구되는 사례, 사용자의 안전을 위한 ’사용방법‘ 및 ’사용 시 주의사항‘ 기재사항 안내 등이다. 또 업체 면담 및 옴부즈만 제도를 통해 적극 수렴한 결과를 반영했다.
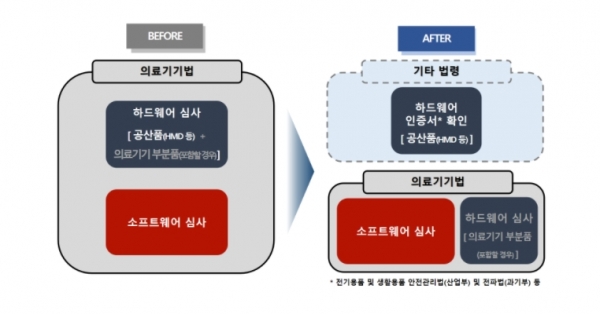
전기를 사용하는 의료기기의 경우 전기 및 전자파 안전에 관한 자료를 의무적으로 제출해야 했으나 가상·증강현실 소프트웨어가 ‘헤드 마운트 디스플레이(HMD)’ 및 모바일기기 등 공산품에 사용될 경우 산품은 타 법령에 따라 발급된 안전 인증서 유무만 확인하고 의료기기에 해당하는 소프트웨어만 심사하도록 개선한다.
이어 업체가 가장 많이 부담을 느끼는 임상시험 분야와 관련해서는 임상시험이 요구되는 사례를 명확히 제시하고 새로운 장치를 사용하더라도 임상시험이 면제되는 사례도 안내한다.
아울러 의료기기 사용자의 안전을 위해 사용 전 소독 및 환자 사용 시 주의사항 등 ‘사용방법’과 ‘사용 시 주의사항’에 반드시 기재해야 할 정보를 구체적으로 제시한다.
식약처는 "이번 가이드라인을 통해 첨단기술이 적용된 의료기기가 신속하게 허가될 수 있을 것으로 기대하며, 앞으로도 새로운 의료기기 특성을 반영한 안내서 등을 지속 발간할 계획"이라고 밝혔다.